Kuinka löytää protonien, elektronien ja neutronien lukumäärä
Kirjoittaja:
Roger Morrison
Luomispäivä:
27 Syyskuu 2021
Päivityspäivä:
1 Heinäkuu 2024

Sisältö
- vaiheet
- Osa 1 Laske protonien, elektronien ja neutronien lukumäärä
- Osa 2 Laske elektronien lukumäärä ionissa
Neutronit, elektronit ja protonit ovat kolme päähiukkasta, jotka muodostavat atomin. Kuten voidaan arvata, protoneilla on positiivinen varaus, elektronilla on negatiivinen varaus ja neutronit ovat vain neutraaleja hiukkasia. Elektronien massa on hyvin pieni. Neutronilla ja protoneilla on kuitenkin samanlaiset massat. Atomin protonien, elektronien ja neutronien lukumäärän löytämiseksi riittää tutustua elementtien jaksotaulukkoon, jota kutsutaan myös Mendelejevin taulukkoksi.
vaiheet
Osa 1 Laske protonien, elektronien ja neutronien lukumäärä
-
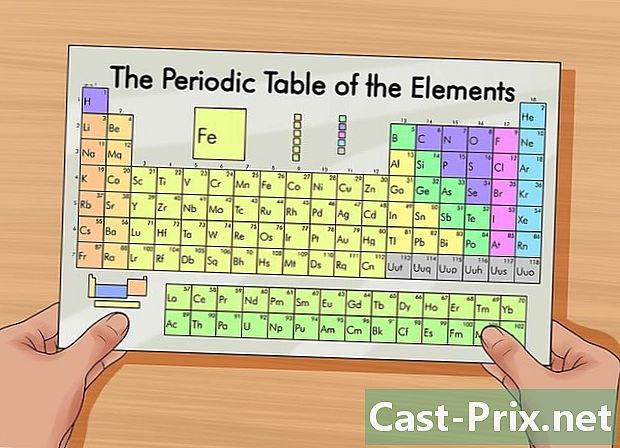
Hanki jaksoittainen tavaroiden taulukko. Tämä taulukko auttaa sinua löytämään protonien, elektronien ja neutronien lukumäärän elementissä. Se on taulukko, joka esittää elementit atomien rakenteen mukaan. Värikoodi erottaa elementit. Jokainen elementti tunnistetaan symbolilla, joka käsittää yhden, kaksi tai kolme kirjainta. Taulukko näyttää myös muita tietoja, kuten atomimassan ja kunkin elementin atominumeron.- Löydät tämän kaavion joko tekemällä haun Internetistä tai kemiankirjasta.
- Tutkimuksissa saa yleensä käyttää jaksollista elementtiä.
-
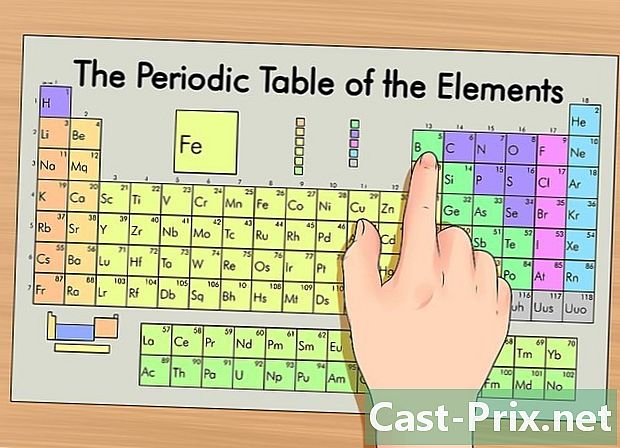
Tunnista elementti jaksotaulukossa. Taulukossa elementit on ryhmitelty atominumeronsa perusteella. Ne on jaettu kolmeen pääryhmään: metallit, ei-metallit ja metalloidit (puolimetallit). Muihin ryhmiin kuuluvat alkalimetallit, halogeenit ja jalokaasut.- Elementti on helpompi paikantaa taulukossa käyttämällä ryhmää (sarake) tai pistettä (rivi).
- Jos et tiedä elementin ominaisuuksia, voit etsiä sen symbolia.
-
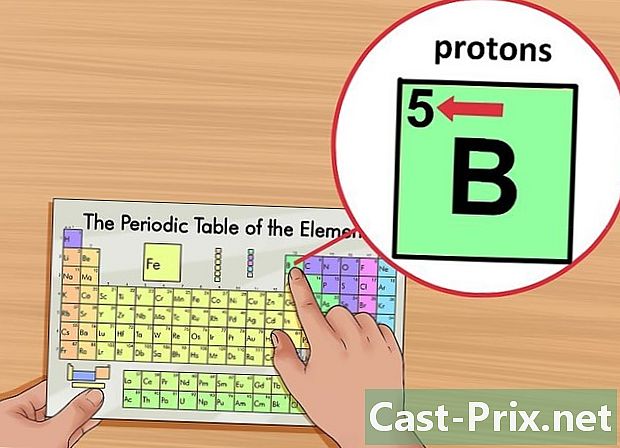
Etsi elementin atominumero. Tämä numero on merkitty ruudun vasempaan yläkulmaan elementtisymbolin yläpuolelle. Atomiluku antaa sinulle protonien lukumäärän, jotka muodostavat kyseisen elementin.- Esimerkiksi boorin (B) atomiluku on 5. Joten sillä on 5 protonia.
-

Määritä elektronien lukumäärä. Atomin ydin sisältää protoneja, jotka ovat positiivisesti varautuneita hiukkasia. Elektronit ovat negatiivisesti varautuneita hiukkasia. Siksi neutraalien elementtien protonien ja elektronien lukumäärä on sama.- Esimerkiksi boorin (B) atomiluku on 5, joten siinä on 5 protonia ja 5 elektronia.
- Kuitenkin, jos se on positiivinen tai negatiivinen ioni, protonien lukumäärä ja elektronien lukumäärä ovat erilaiset. Sinun on laskettava ne. Leijonanvaraus ilmoitetaan pienellä painotuotteella vastaavan esineen jälkeen.
-

Etsi alkuaineen atomimassa. Tämän vaiheen avulla voit löytää neutronien lukumäärän. Ensin on määritettävä elementin atomimassa tai atomipaino. Tämä nollapiste edustaa tämän elementin atomien keskimääräistä massaa. Se on kirjoitettu elementin symbolin alle.- Pyöristä elementin atomimassa lähimpään kokonaislukuun. Boorin atomimassa on siis 10.811, mutta sinun on vieritettävä arvoon 11.
-

Tee ero atomiluvun ja atomimassan välillä. Neutronien lukumäärän laskemiseksi sinun on erotettava atomiluku ja atomimassa. Älä unohda, että tunnet jo atominumeron. Se on yksinkertaisesti identtinen protonien kanssa.- Boorin tapauksessa sinulla on: 11 (atomimassa) - 5 (atominumero) = 6 neutronia
Osa 2 Laske elektronien lukumäärä ionissa
-

Löydä ionin sähkövaraus. Tämä numero näkyy eksponentilla elementtisymbolin jälkeen. Ioni on atomi, jolla on positiivinen tai negatiivinen varaus johtuen elektronien lisäyksestä tai tukahduttamisesta. Protonien lukumäärä atomissa ei vaihtele. Ionissa elektronien lukumäärä kuitenkin muuttuu.- Koska elektronilla on negatiivinen varaus, se muuttuu positiiviseksi yhden tai useamman elektronin poistamisen jälkeen. Toisaalta, elektronien lisäämisellä on vaikutusta, että varaus on negatiivinen.
- Esimerkiksi N: n kuorma on -3. Toisaalta Ca: n arvo on +2.
- Älä unohda, että laskenta ei ole välttämätöntä, jos elementin symbolia ei seuraa eksponentti.
-

Poista varaus atominumerosta. Alun perin positiivisella varauksella oleva ioni on atomi, joka on menettänyt elektroneja. Elektronien lukumäärän löytämiseksi sinun on vähennettävä ylimääräiset varaukset atominumerosta. Jos leijona on positiivinen, protonien lukumäärä on suurempi kuin elektronien.- Esimerkiksi Ca: n varaus on +2. Seurauksena hän menetti 2 elektronia alkuperäiseen tilaansa verrattuna. Kalsiumin atominumero on yhtä suuri kuin 20, joten leijonalla on 18 elektronia.
-

Lisää varaus negatiivisten ionien atomimäärään. Kun ioni on negatiivisesti varautunut, latomilla on ylimääräisiä elektroneja. Elektronien kokonaismäärän laskemiseksi riittää, että lisätään ylimääräisten varausten lukumäärä atominumeroon. Jos leijona on negatiivinen, hänellä on vähemmän protoneja kuin elektronilla.- Esimerkiksi N: n kuorma on -3. Joten, se kantaa 3 enemmän elektronia alkuperäiseen tilaansa verrattuna. Latsotin atomiluku on 7. Siksi tässä ionissa on 10 elektronia.

